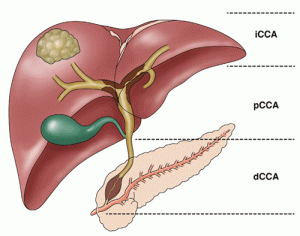
Incyte ha annunciato che il Comitato per i medicinali per uso umano (CHMP) dell’Agenzia europea per i medicinali (EMA) ha emesso un’opinione positiva, raccomandando l’autorizzazione all’immissione in commercio condizionale di pemigatinib per il trattamento di adulti con colangiocarcinoma non resecabile localmente avanzato o metastatico con fusione o riarrangiamento del recettore 2 del fattore di crescita dei fibroblasti (FGFR2), recidivante o refrattario dopo almeno una prima linea di terapia sistemica. Se approvato, pemigatinib sarà la prima terapia mirata nell’Unione europea per questa indicazione.
Cerca articoli
Articoli recenti
- ESEO Italia: al via la campagna di sensibilizzazione per le patologie gastrointestinali eosinofile
- Prevenzione cardiovascolare 3.0: dalle pietre miliari ai nuovi fattori di rischio
- Malattie rare, al via l’Osservatorio sui nutraceutici
- Parse Biosciences lancia prodotti di profilazione immunitaria a cellula singola
- Melanoma day: troppe diagnosi tardive